Acetato de sodio trihidrato, también conocido como "acetato de sodio trihidrato", es un importante material químico de partida con aplicaciones y significado extensos. Se utiliza principalmente como agente de fusión, coagulante y anticascaras, siendo capaz de estabilizar el pH y regular la acidez y alcalinidad. El acetato de sodio trihidrato tiene numerosas funciones y usos. En el campo químico, se utiliza para preparar y formular soluciones de buffer y como conservante y limpiador ácido. Su papel ayuda a mantener los alimentos en valores específicos de pH y prevenir el crecimiento de bacterias perjudiciales. En el campo farmacéutico, es un importante excipiente farmacéutico, ampliamente utilizado en la producción de cuidado bucal y detergentes. Además, en la salud oral, el acetato de sodio trihidrato prefiere prevenir la caries dental, limpia la boca, elimina manchas y desinfecta. También encuentra aplicaciones amplias en la producción de fuegos artificiales, aditivos alimentarios y más.
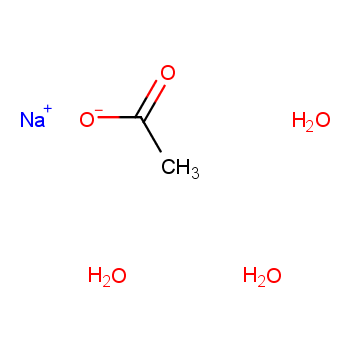
El acetato de sodio trihidrato, a menudo abreviado como SAT, es un compuesto cristalino con la fórmula química CH3COONa·3H2O. Se forma por la combinación de moléculas de acetato de sodio y tres moléculas de agua, por lo que se le llama "trihidrato".
El acetato de sodio trihidrato consta de iones de sodio (Na+), iones de acetato (CH3COO-) y moléculas de agua (H2O). Los iones de sodio actúan como cátions, mientras que los iones de acetato actúan como ánions, formando un compuesto ionic estable.
El acetato de sodio trihidrato encuentra aplicaciones amplias en diversas industrias, incluyendo farmacéuticos como agente de buffer, aditivos alimentarios, bolsas de calor y un componente clave en la demostración de "hielo caliente". Sus propiedades únicas hacen que sea un valioso sustancia para los experimentos científicos y las aplicaciones prácticas.
Actualmente, las rutas tecnológicas para la producción de acetato de sodio trihidrato (SAT) utilizadas en el país y en el extranjero se clasifican en dos categorías según los materiales básicos de alcalinos utilizados: uno utilizando hidróxido de sodio como material básico, y el otro utilizando carburo de sodio. Según el tipo de ácido acético utilizado, se clasifica en ácido acético puro y ácido acético diluido reciclado. El proceso de producción de acetato de sodio trihidrato (SAT) implica varios pasos complejos para asegurar la producción de altas calidad de cristales. A continuación, profundizaremos en los procedimientos intricados requeridos para sintetizar SAT a gran escala:

ácido acético: El ácido acético es el precursor clave para la producción de SAT. Hidróxido de sodio (NaOH): El hidróxido de sodio, también conocido como soda cáustica, es otro importante material básico.
Se mezcla cuidadosamente el ácido acético con el hidróxido de sodio en un ambiente controlado para producir acetato de sodio y agua. La reacción se monitorea de cerca para garantizar una proporción correcta y un nivel de pH adecuado.
La solución de acetato de sodio obtenida de la reacción neutralizadora se somete a la cristalización. La cristalización se puede inducir a través de varios métodos como enfriamiento, evaporación o sembramiento, dependiendo del dise?o de fabricación específico. Los parámetros controlados incluyen la temperatura, la presión y la agitación, son cruciales para promover la formación de altas calidad de los cristales SAT.
Después de la cristalización, los cristales de acetato de sodio purificados se separan de la lúpulo madre. Las técnicas de separación pueden incluir filtración, centrifugación o decantación para separar los cristales de acetato de sodio de la fase líquida. Los cristales separados se someten a procesos de lavado y secado para eliminar impurezas y exceso de humedad, asegurando la pureza y la estabilidad del producto.
Los cristales purificados de acetato de sodio trihidrato se empaquetan entonces en contenedores apropiados como bolsas o barriles y se distribuyen a los usuarios finales. Es necesario un correcto etiquetado y documentación para cumplir con los estándares regulatorios y asegurar el manejo seguro durante el transporte y almacenamiento.
Hacer acetato de sodio trihidratado (SAT) en casa es un experimento interesante que se puede realizar utilizando artículos domésticos de fácil acceso. Aquí tienes una guía detallada que describe el proceso paso a paso:
Vierte el vinagre blanco medido en el contenedor resistente al calor. La cantidad exacta dependerá de la cantidad de SAT necesaria.
Agrega lentamente bicarbonato de sodio al vinagre mientras remueves continuamente. La reacción entre el vinagre y el bicarbonato de sodio producirá una solución de acetato de sodio, agua y gas dióxido de carbono. Revuelve hasta que no se formen más burbujas.
Coloca el contenedor con la solución de acetato de sodio en la estufa o placa caliente. Calienta la solución suavemente a fuego bajo a medio para permitir que el agua se evapore lentamente. Revuelve la solución ocasionalmente para evitar una evaporación desigual.
Continúa calentando hasta cerca de la temperatura de ebullición, pero evita la ebullición vigorosa. Una vez que la mayor parte del agua se haya evaporado, retira el contenedor del calor y deja enfriar ligeramente. A medida que la solución se enfría, comenzarán a formarse los cristales de acetato de sodio trihidratado. Puede observarse la nucleación o formación de cristales semilla.
Una vez que la solución se enfríe a temperatura ambiente, filtra la mezcla utilizando papel de filtro o filtro de café para separar los cristales del líquido restante. Transfiere los cristales filtrados a una superficie limpia y déjalos secar al aire completamente. Evita la exposición a la humedad durante el proceso de secado.
Después de secar, almacena los cristales de SAT en un recipiente sellado para evitar que absorban la humedad del entorno. Etiqueta el recipiente con la fecha de producción e instrucciones adecuadas para su manejo.
Siguiendo estos simples pasos, puedes preparar con éxito acetato de sodio trihidratado en casa.
Este artículo presentará el método de producción de acetato de sodio trihidratado utilizando ácido acético del residuo de oxidación del ácido tereftálico, con los pasos específicos como sigue:
La madre licor que contiene cobalto y manganeso recuperado del taller de recuperación del residuo de oxidación de PTA se introduce en el alambique de destilación y se destila bajo agitación y presión reducida para destilar ácido acético. La velocidad de agitación es de 60 a 80 rpm, el grado de vacío es de -0.04 a -0.09 Mpa, y la temperatura del alambique es de 60 a 85 °C. El propósito de este paso es que el ácido acético diluido utilizado como materia prima para la síntesis de SAT se recupere del residuo de oxidación de PTA, que contiene una gran cantidad de ácido benzoico. Si se sintetiza directamente el acetato de sodio trihidratado, el producto contendrá impurezas de sodio benzoico, afectando la pureza del producto. Por lo tanto, la purificación del ácido acético diluido se convierte en un requisito previo para todo el proceso de síntesis de acetato de sodio. En este proceso de separación, una tecnología clave muy importante es comenzar desde la purificación del ácido acético diluido, es decir, separar el residuo de oxidación de PTA en ácidos orgánicos insolubles. Después, bajo alto vacío (-0.085Mpa o más), es decir, bajo la condición de que la temperatura del alambique no supere los 65 °C, para evitar la sublimación del ácido benzoico. Además, utilizando la baja solubilidad del ácido benzoico en ácido acético diluido, se reduce el ácido acético diluido a temperatura ambiente para una separación adicional, obteniendo así ácido acético diluido de alta pureza.
El ácido acético diluido purificado se introduce en el alambique de reacción y se neutraliza lentamente con álcali bajo agitación y refrigeración por agua. La velocidad de agitación es de 60 a 80 rpm, la temperatura de reacción es de 60 a 70 °C, y el pH final se controla entre 6.0 y 7.0. Durante la reacción, la materia prima que se obtiene es acetato de sodio.
La solución de reacción de acetato de sodio después de la neutralización se introduce en el alambique de destilación y se calienta para evaporar bajo agitación y a presión reducida. La velocidad de agitación es de 60 a 80 rpm, el grado de vacío es de -0.05 a -0.08 Mpa, la temperatura del alambique es de 65 a 80°C, y cuando la concentración de ácido acético alcanza el 80%, se mide el valor de pH de la solución. Cuando el valor de pH supera 9, se acidifica la solución de reacción de acetato de sodio hasta que el valor final de pH esté entre 7.5 y 9.
Enfríe la solución de reacción evaporada y concentrada a 70-80°C, luego viértala en un filtro para su filtración. El filtrado entra en el alambique de reacción, y el residuo filtrado es acetato de sodio. El propósito de este paso es que la solución de reacción concentrada después de la concentración al vacío contiene trazas de impurezas de benzoato de sodio, por lo que en un proceso de cristalización simple y eliminación de impurezas se utiliza eficazmente el principio de la diferencia en solubilidad entre el trihidrato de acetato de sodio y el benzoato de sodio a una cierta temperatura y sus diferencias en cristalización para separarlos, es decir, cuando la solución de reacción se concentra a una concentración del 80-85%, y la temperatura es de 70-80°C, el ácido benzoico como impureza precipita gradualmente, mientras que el acetato de sodio no puede precipitar debido a su alta solubilidad sin la adición de cristales de semilla. En este caso, se realiza una filtración en caliente. Si la temperatura de filtración es demasiado baja, la concentración de sobresaturación del acetato de sodio es demasiado alta, el estado de la solución es muy inestable, una ligera vibración o fricción inducirá cristalización, y el benzoato de sodio filtrado contendrá una gran cantidad de acetato de sodio, lo que resultará en un fallo de separación. Por lo tanto, en el proceso de eliminación de impurezas, la concentración de sobresaturación de la solución y la temperatura de filtración son las condiciones clave para la separación efectiva del acetato de sodio y el benzoato de sodio.
Agite y enfríe el alambique de reacción filtrado a una temperatura de 53-57°C, a?ada el 1% de la cantidad teórica de acetato de sodio al filtrado como un indutor de cristalización, y controle el tiempo de enfriamiento a 4-5 horas. Después de enfriar a temperatura ambiente, viértalo en un filtro hasta que esté seco. Después del secado, el licor madre se devuelve al alambique de destilación para su reutilización, y el residuo filtrado es trihidrato de acetato de sodio húmedo.
Coloque el trihidrato de acetato de sodio húmedo en un secador al vacío para su secado al vacío. El grado de vacío es de -0.085 a -0.09 Mpa, y la temperatura es de 35 a 40°C. Cuando se seque hasta un valor constante, se obtiene el producto.
El trihidrato de acetato de sodio (SAT) posee notables habilidades transformadoras, capaces de convertirse en hielo caliente, que se puede utilizar para crear demostraciones cautivadoras. A continuación, exploraremos el proceso de producción de hielo caliente utilizando SAT:
Comience disolviendo cristales de trihidrato de acetato de sodio en agua destilada para formar una solución saturada. Asegúrese de que la solución esté calentada ligeramente por debajo de su punto de ebullición para maximizar la solubilidad.
Introduzca un agente nucleante en la solución caliente de acetato de sodio para activar la cristalización. Esto se puede lograr agregando un peque?o cristal de SAT, un cristal de semilla o raspando cuidadosamente la superficie del recipiente.
A medida que la solución se enfría, las moléculas de acetato de sodio comienzan a reorganizarse en una estructura cristalina sólida. Este proceso libera calor latente, haciendo que la solución se solidifique rápidamente en una masa de sustancia cristalina transparente.
La cristalización del trihidrato de acetato de sodio es un proceso exotérmico, lo que significa que libera energía térmica. Cuando se forma el hielo caliente, genera un aumento notable de temperatura, de ahí su nombre.
Una vez formado, el hielo caliente puede moldearse en diversas formas y estructuras utilizando herramientas o moldes. Su maleabilidad permite una experimentación creativa y expresión artística.
El trihidrato de acetato de sodio es un compuesto químico que se disuelve fácilmente en agua, pero también es propenso a la deliquescencia, lo que requiere un almacenamiento sellado y seco. Se deben tomar medidas de protección al almacenar y transferir trihidrato de acetato de sodio, como usar recipientes sellados o materiales de embalaje para prevenir la exposición al aire y la posterior deliquescencia. Al manipular, se deben usar equipos de protección adecuados, como guantes y gafas de seguridad, para evitar el contacto directo con la sustancia química.
El trihidrato de acetato de sodio también es una sustancia no tóxica. No obstante, debe evitarse el contacto con los ojos y la ingestión. Si se producen derrames, se deben limpiar inmediatamente utilizando métodos de limpieza seguros y efectivos. Para cualquier síntoma de irritación o malestar, se recomienda buscar atención médica.
El acetato de sodio trihidratado se puede hacer fácilmente en casa utilizando vinagre (ácido acético) y bicarbonato de sodio (bicarbonato sódico). Simplemente mezcla vinagre y bicarbonato de sodio para iniciar una reacción de neutralización, luego evapora la solución para permitir que se formen cristales.
Para hacer hielo caliente, primero prepara una solución saturada de acetato de sodio trihidratado en agua destilada. Calienta la solución cerca de su punto de ebullición, luego introduce un agente nucleante para iniciar la cristalización. A medida que la solución se enfría, se solidifica en hielo caliente, liberando calor en el proceso.
Aunque el hielo caliente es conocido principalmente por su atractivo visual y su valor educativo, también tiene aplicaciones prácticas. Se puede utilizar como calentadores de manos, paquetes de calor reutilizables e incluso en ciertas reacciones químicas donde se necesita una liberación controlada de calor.
El acetato de sodio trihidratado y el hielo caliente son generalmente seguros de manejar. Sin embargo, se debe tener precaución al trabajar con líquidos calientes y objetos afilados durante la preparación y el manejo. Asegúrate de contar con una ventilación adecuada y utiliza recipientes resistentes al calor para evitar quemaduras o lesiones.
El acetato de sodio trihidratado es un compuesto químico versátil. Desde detergentes de lavandería domésticos hasta aditivos alimentarios, y desde adyuvantes antibióticos en medicina hasta biomateriales para reparación, el acetato de sodio deja su huella. El acetato de sodio trihidratado abre puertas a posibilidades infinitas y exploración creativa. Desde sus simples orígenes como compuesto hasta sus propiedades transformadoras en la creación de hielo caliente, SAT ofrece un fascinante viaje en los reinos de la química y el arte.
Por lo tanto, ya sea en la ciencia experimental o en la vida cotidiana, el acetato de sodio trihidratado seguirá siendo una herramienta esencial para explorar lo desconocido, aprovechando sus propiedades químicas y las mágicas habilidades de sus reacciones. Exploremos este campo con audacia y creatividad, desatando nuestro potencial para crear más con acetato de sodio trihidratado.
[1]CN200810229404.2
[2] Wang Qinzheng. Investigación sobre el sobreenfriamiento y la estabilidad cíclica del acetato de sodio trihidratado [D]. Universidad de Ciencia y Tecnología de Huazhong, 2021. DOI:10.27157/d.cnki.ghzku.2021.001874.
 |
 |
 |