El uso combinado de fludarabina y ciclofosfamida ha atraído una considerable atención en el tratamiento de las malignidades hematológicas. Numerosos estudios han explorado la eficacia y seguridad de estos dos medicamentos en combinación, particularmente en el tratamiento de la leucemia linfocítica crónica (LLC). La fludarabina, un análogo de nucleósido purínico, interrumpe la síntesis y reparación del ADN, inhibiendo así la proliferación de células cancerosas, mientras que la ciclofosfamida, un agente alquilante, mata las células cancerosas al formar enlaces cruzados en el ADN.

La fludarabina pertenece a una clase de medicamentos conocidos como antimetabolitos y se utiliza en el tratamiento de un cáncer llamado leucemia linfocítica crónica (LLC) de células B. Se emplea en pacientes con LLC que han recibido tratamiento previo con un agente alquilante como la bendamustina, pero que han mostrado una respuesta insuficiente.
La fludarabina interrumpe el crecimiento de las células cancerosas, lo que finalmente conduce a su destrucción. Sin embargo, también puede afectar el crecimiento de las células normales, lo que conlleva efectos secundarios potenciales. Algunos de estos efectos secundarios pueden ser graves y deben ser informados a un médico, mientras que otros pueden ser menos graves pero aún preocupantes. Algunos efectos secundarios pueden persistir incluso después de interrumpir el tratamiento con fludarabina. Antes de comenzar el tratamiento con fludarabina, usted y su médico deben discutir los beneficios y riesgos de este medicamento. La fludarabina solo debe ser utilizada bajo prescripción médica. La fludarabina oral fue retirada del mercado de EE. UU. en septiembre de 2011.
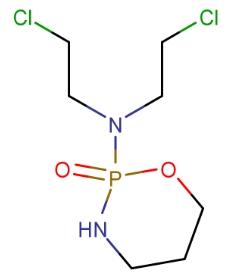
La ciclofosfamida es un precursor de los agentes alquilantes y debe ser activada en el hígado para formar fosforamida activa. Se ha utilizado en el tratamiento de linfomas y leucemias. Sus efectos secundarios incluyen la pérdida de cabello, y ha sido utilizada para "depilar" ovejas. La ciclofosfamida también puede causar infertilidad, defectos de nacimiento, mutaciones y cáncer.
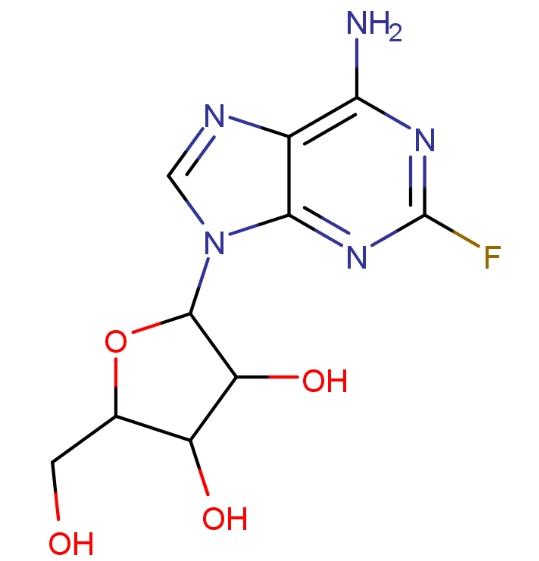
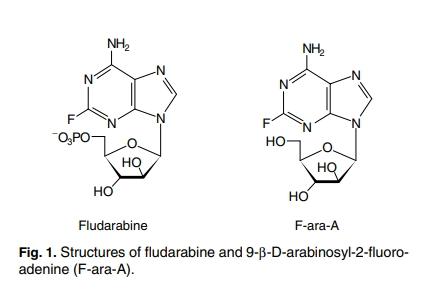
La fludarabina es un medicamento de quimioterapia utilizado en el tratamiento de la leucemia linfocítica crónica (LLC). Actúa sobre la ADN polimerasa α, la ribonucleótido reductasa y la ADN primasa, inhibiendo la síntesis de ADN y alterando las células cancerosas.
La fludarabina fosforilada se desfosforila rápidamente a 2-fluoro-ara-A, que luego se somete a fosforilación intracelular por la deoxicitosina quinasa a la sal activa de triphosphato 2-fluoro-ara-ATP. Este metabolito parece actuar inhibiendo la ADN polimerasa α, la ribonucleótido reductasa y la ADN primasa, suprimiendo así la síntesis de ADN. El mecanismo exacto de acción de este antimetabolito no se entiende completamente y puede involucrar varios aspectos.
La ciclofosfamida es un medicamento anticancerígeno perteneciente a la clase de los agentes alquilantes, utilizado para tratar diversos cánceres. Los agentes alquilantes reciben su nombre porque pueden a?adir grupos alquilo a muchos grupos electronegativos en las células. Previenen el crecimiento del tumor mediante la formación de enlaces cruzados entre las bases de guanina en la doble hélice de ADN (ataque directo al ADN), evitando que las hebras se desenrollen y separen. Dado que esto es necesario para la replicación del ADN, las células no pueden dividirse. Además, estos medicamentos a?aden metilo u otros grupos alquilo a moléculas a las que no pertenecen, lo que a su vez impide su correcta utilización mediante emparejamiento de bases, lo que lleva a errores de codificación del ADN. Los agentes alquilantes son inespecíficos en el ciclo celular. Los agentes alquilantes actúan a través de tres mecanismos diferentes, todos los cuales logran el mismo resultado final: la alteración de la función del ADN y la muerte celular.
La fludarabina se utiliza principalmente para tratar la leucemia linfocítica crónica de células B y el linfoma no Hodgkin. Es un medicamento anticanceroso eficaz y bien tolerado que ha sido estudiado en varias malignidades linfoproliferativas. La fludarabina es una opción de tratamiento eficaz para la terapia de segunda línea en la leucemia linfocítica crónica avanzada. Los datos de estudios comparativos recientes también apoyan su uso temprano en pacientes con leucemia linfocítica crónica que no han recibido quimioterapia previa. Además, la evidencia emergente de estudios existentes enfatiza cada vez más el papel significativo de la fludarabina en el tratamiento de leucemia aguda y linfoma no Hodgkin de bajo grado, así como posiblemente otras enfermedades linfoproliferativas, especialmente cuando se usa como parte de una quimioterapia combinada.
La inyección intravenosa de ciclofosfamida se utiliza para tratar varios tumores malignos, incluyendo linfoma de Hodgkin, linfoma linfoblástico, linfoma de células mixtas, linfoma histiocítico, linfoma de Burkitt, mieloma múltiple, leucemia, infecciones por hongos, neuroblastoma, adenocarcinoma de ovario, retinoblastoma y cáncer de mama. Las cápsulas orales de ciclofosfamida también se usan para tratar el síndrome nefrótico pediátrico que no responde (o es intolerante) a la terapia con corticosteroides.
Eficacia Clínica de la Terapia Combinada de Fludarabina y Ciclofosfamida:
FCR es una combinación de medicamentos anticancerosos utilizada para tratar la leucemia linfocítica crónica (LLC). FCR ha mostrado los mejores resultados en términos de tasa de CR, PFS y OS para los pacientes con LLC recién diagnosticados hasta la fecha. Está compuesta por los siguientes medicamentos: fludarabina, ciclofosfamida y rituximab.
La fludarabina es un análogo de nucleósido purina fluorada resistente a la adenosina desaminasa, estudiada inicialmente como un agente único en pacientes con LLC en recaída/refractarios (R/R), con tasas de respuesta que varían entre 33-57%. En pacientes no tratados previamente, la tasa de respuesta general (ORR) a la fludarabina como monoterapia puede ser tan alta como el 70%.
Para mejorar las tasas de respuesta del tratamiento con fludarabina sola y basándose en evidencia in vitro de la sinergia entre fludarabina y ciclofosfamida [Yamauchi et al., 2001], se realizó una prueba de tratamiento de LLC con la combinación de ambos medicamentos (FC), incluyendo pacientes previamente tratados solo con fludarabina. Un total de 128 pacientes con LLC recibieron diversos tratamientos con el régimen FC. La tasa de respuesta general a fludarabina o agentes alquilantes al inicio del estudio fue mayor o igual al 80%. Se demostró más evidencia de sinergia entre ambos medicamentos, con pacientes resistentes a la fludarabina al inicio del estudio aún logrando una tasa de respuesta del 38% con la terapia combinada FC. Sin embargo, la tasa de respuesta completa (CR) siguió siendo baja, con un 35% para los pacientes no tratados previamente.
El régimen FCR fue inicialmente evaluado por el equipo de MD Anderson en un ensayo de fase II en pacientes con LLC R/R. El régimen incluía rituximab 375 mg/m2 (día 1 del ciclo 1) y 500 mg/m2 (día 1 de los ciclos 2-6); fludarabina 25 mg/m2/día; y ciclofosfamida 250 mg/m2/día, administrados durante 3 días por ciclo. Según el informe final actualizado de este ensayo, entre 280 pacientes evaluables, el 30% alcanzó CR, el 14% alcanzó remisión parcial nodular (nPR), el 30% alcanzó remisión parcial (PR), y la ORR fue del 74%. Los pacientes que habían recibido 3 o más terapias previas tuvieron tasas de CR y PR significativamente más altas en comparación con aquellos que recibieron 4 o más terapias previas (CR/nPR = 52% vs. 4%, p < 0.0001). Los pacientes tratados previamente con rituximab o fludarabina sola (sin agentes alquilantes) no tuvieron un impacto negativo en las tasas de respuesta (CR/nPR 62% y ORR 84%); sin embargo, los pacientes tratados con fludarabina y agentes alquilantes presentaron tasas de respuesta moderadas (CR/nPR 42% y ORR 73%), con tasas de respuesta significativamente más bajas en pacientes resistentes a la fludarabina en comparación con aquellos que habían respondido a regímenes que contenían fludarabina previamente (CR/nPR = 8% vs. 46%, p = 0.023). La mediana de la supervivencia libre de progresión (PFS) para los pacientes que alcanzaron CR fue de 60 meses, para los pacientes con nPR fue de 38 meses (p = 0.076), y para los pacientes con PR fue de 15 meses (p < 0.001). Los pacientes con anormalidades citogenéticas de alto riesgo (del 17p, del 11q, 3 o más anormalidades citogenéticas) tuvieron una PFS más baja.
Posteriormente, en un ensayo clínico de fase II, el régimen FCR fue evaluado en pacientes con LLC que no habían recibido tratamiento previo. Entre 224 pacientes en este ensayo, la tasa de CR fue del 70%, y la ORR fue del 95%. Las características previas al tratamiento estuvieron significativamente asociadas con una menor probabilidad de CR (p < 0.05), incluyendo el estadio avanzado de Rai y Binet, edad avanzada, mayor recuento de células blancas, menor recuento de plaquetas, mayor nivel de β2-microglobulina sérica, >50% de celularidad en la biopsia de médula ósea, y agrandamiento del bazo >5 cm por debajo del margen costal izquierdo. Se realizó una evaluación por citometría de flujo de la enfermedad residual en aspirados de médula ósea en 207 pacientes, con el 67% de los pacientes mostrando <1% de co-expresión de células CD5 y CD19, considerado "CR por citometría de flujo". Las complicaciones más comunes de este régimen fueron la supresión de la médula ósea y las complicaciones infecciosas. Los resultados más recientes de este ensayo mostraron una tasa de supervivencia global a 6 a?os y una tasa de supervivencia sin fallos de 77% y 51%, respectivamente, con un tiempo medio de progresión de 80 meses.
El ensayo fase III CLL8 fue el primer gran ensayo aleatorizado que comparó la eficacia de FC y FCR en pacientes recién diagnosticados con LLC. De manera abierta, se asignaron aleatoriamente 817 pacientes a uno de los regímenes. Los resultados actualizados recientemente de este ensayo mostraron un tiempo medio de seguimiento de 5.9 a?os, con PFS de 56.8 meses para FCR y 32.9 meses para FC (razón de riesgo (HR), 0.59; intervalo de confianza (CI) del 95%, 0.50–0.69, p < 0.001). Además, la superioridad en términos de OS fue significativa: el grupo FCR no alcanzó OS, mientras que el grupo FC tuvo 86 meses (HR, 0.68; CI del 95%, 0.54–0.89, p = 0.001). Las principales toxicidades asociadas con esta terapia fueron la supresión de la médula ósea (potencialmente prolongada) y las complicaciones infecciosas.
Las interacciones de medicamentos pueden alterar la forma en que los medicamentos funcionan o aumentar el riesgo de efectos secundarios graves. Este documento no contiene todas las posibles interacciones medicamentosas. Mantenga una lista de todos los productos que utiliza (incluidos los medicamentos con receta/sin receta y productos herbales) y compártala con su médico y farmacéutico. No inicie, detenga ni cambie la dosis de ningún medicamento sin la aprobación de su médico.
Si se está utilizando fludarabina y otros medicamentos como pentostatin, cladribina o mercaptopurina, las interacciones de medicamentos pueden ocurrir y aumentarse los efectos adversos, por lo que estos medicamentos no se deben usar juntos a menos que lo indique un médico. No debe utilizarse fludarabina con otros medicamentos que disminuyan la función de la médula ósea (como la zidovudina) porque esto puede causar una supresión de la médula ósea grave.
Revise cuidadosamente todas las etiquetas de los medicamentos recetados y de venta libre, ya que muchas contienen analgésicos/antipiréticos (como los antiinflamatorios no esteroides como el ibuprofeno, naproxeno y aspirina), los cuales pueden aumentar el riesgo de sangrados. Si el medicamento recetado por su médico es para prevenir infartos o accidentes cerebrovasculares, continúe tomando aspirina en dosis bajas (generalmente 81-162 miligramos por día). Consulte a su médico o farmacéutico para más detalles.
La investigación sobre el uso combinado de fludarabina y ciclofosfamida indica una eficacia significativa en el tratamiento de la leucemia linfocítica crónica (LLC). Muchos ensayos clínicos y hallazgos de investigación respaldan sus ventajas para mejorar las tasas de respuesta, extender la supervivencia libre de progresión y la supervivencia global. Sin embargo, estos estudios también destacan los posibles efectos secundarios y riesgos asociados con la terapia combinada. Por lo tanto, en la aplicación clínica práctica, los médicos deben sopesar los beneficios y riesgos y adaptar el plan de tratamiento más adecuado para cada paciente individual. En el futuro, con más investigaciones y la aparición de nuevas terapias, se explorará aún más el potencial de combinar fludarabina y ciclofosfamida, brindando más esperanza y opciones a los pacientes.
[1]https://go.drugbank.com/drugs/DB01073
[2]https://go.drugbank.com/drugs/DB00531
[3]https://link.springer.com/article/10.1007/s12185-022-03488-5
[4]https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5305006/
[5]https://www.ncbi.nlm.nih.gov/books/NBK304336/
[6]https://www.webmd.com/drugs/2/drug-8784/fludarabine-intravenous/details
[7]https://www.cancerresearchuk.org/about-cancer/treatment/drugs/fcr
 |
 |
 |