
ルイス構(gòu)造はギルバート?N?ルイスによって考案され、分子內(nèi)の電子の配置を視覚的に表現(xiàn)します。価電子を點(diǎn)で、共有結(jié)合を線で示すことで、八隅則に基づいて分子の形狀や性質(zhì)を予測します。この八隅則は、原子が外殻に8つの電子を持つことで安定を得ようとする性質(zhì)を表します。ルイス構(gòu)造はこの規(guī)則に従っており、化學(xué)結(jié)合の明確なイメージを提供します。
メチル基(CH3)は、1つの炭素原子が3つの水素原子と結(jié)合した一価の官能基です。有機(jī)化合物に一般的に存在し、さまざまな化學(xué)反応や生物學(xué)的プロセスにおいて重要な役割を果たします。八隅則を完全には満たしていないにもかかわらず、電子の共有によって安定化されています。

CH3 のルイス構(gòu)造を描く手順を見ていきましょう:
ステップ1:中心原子の特定:炭素(C)は水素よりも電気陰性度が低いため、CH3 の中心原子です。
ステップ2:価電子の合計を計算:炭素は4個、水素は1個ずつで、合計4 + (3 x 1) = 7個の価電子になります。
ステップ3:原子の周りに電子を配置:水素原子を炭素原子に単結(jié)合で結(jié)び、殘りの電子を炭素の孤立電子対として配置します。
ステップ4:八隅則を満たす:炭素が8個、水素がそれぞれ2個の電子を持つようにします。
ステップ5:形式電荷の確認(rèn):全ての原子が八隅則を満たしていれば、形式電荷は必要ありません。
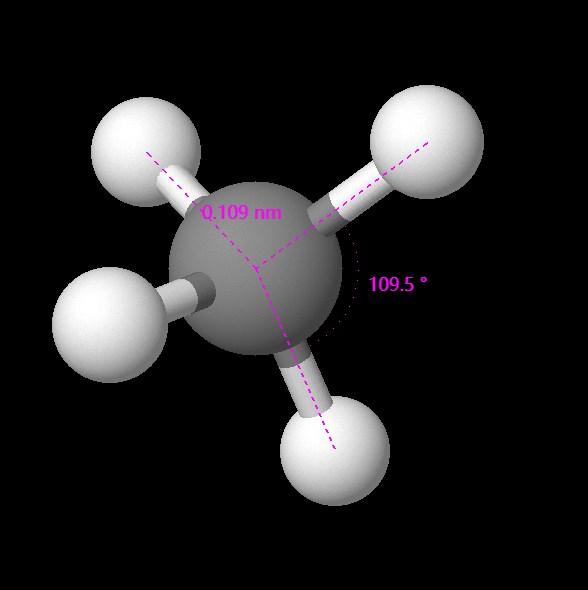
メチル基(CH3)は中心の炭素原子の周囲に8個の電子(または4つの電子対)があります。そのうち1つは孤立電子対です。このため、CH3 の分子構(gòu)造は三角錐形(trigonal planar)になります。H-C-H の結(jié)合角は109.5度になります。
この理論は、電子反発や安定な構(gòu)造の必要性を説明します。CH3 では、炭素と水素の間に3つのシグマ結(jié)合が形成され、炭素に1つの孤立電子対があります。分子軌道理論は、結(jié)合および非結(jié)合の相互作用を説明し、安定した構(gòu)造を形成します。
ルイス構(gòu)造により、CH3 は三角錐形を取ると示されます。この構(gòu)造では、3つの水素原子が中心の炭素原子の周囲に対稱に配置され、3つの結(jié)合対を形成します。この形狀は電子間反発を最小限に抑え、安定な構(gòu)造となります。
炭素と水素の相互作用によって関與する軌道と形成される結(jié)合を調(diào)べて、メチル基(CH3)の混成を決定します。2s、2px、2py、2pz 軌道が関與します。炭素原子は基底狀態(tài)で 2s22p2 の配置を持ち、勵起狀態(tài)では 2s と 2px の電子対が対を解かれ、それぞれ 2py と 2pz に遷移します。これにより 1つの 2s と 3つの 2p 軌道が混成し、4つの sp3 混成軌道が形成されます。
CH3 の結(jié)合角はおおよそ109.5度です。この角度は、分子が三角錐形であり、水素原子が炭素の周囲に等間隔で配置されているためです。結(jié)合長は約109.2ピコメートル(pm)です。
| メチル基(CH3) | |
| 分子式 | CH3 |
| 分子形狀 | 三角錐形 |
| 極性 | 無極性 |
| 混成軌道 | sp3 混成 |
| 結(jié)合角 | 109.5 度 |
| 結(jié)合長 | 109.2 pm |
ルイス構(gòu)造の極性を判斷するには、分子構(gòu)造と結(jié)合の極性を確認(rèn)します。メチル基(CH3)の場合、炭素が中心にあり、3つの水素原子が結(jié)合しています。CH3 は三角錐形で、水素原子が対稱に配置されています。C-H 結(jié)合は極性を持ちますが、分子の対稱性により雙極子モーメントが打ち消され、CH3 は無極性分子になります。
CH3 の総結(jié)合エネルギーを求めるには、まずC-H単結(jié)合のエネルギー(約413 kJ/mol)を調(diào)べ、それを結(jié)合數(shù)で掛けます。CH3 は3つのC-H結(jié)合があるため、413 × 3 = 1239 kJ/mol になります。これは、1モルのCH3 分子のすべてのC-H結(jié)合を切斷するのに必要なエネルギーです。
結(jié)合次數(shù)は、原子間に存在する結(jié)合の數(shù)を示します。CH3 のルイス構(gòu)造では、各C-H結(jié)合は単結(jié)合なので、各C-H結(jié)合の結(jié)合次數(shù)は1です。共鳴構(gòu)造を持つ分子では平均を取る必要がありますが、CH3 に共鳴はないため、結(jié)合次數(shù)はそのまま1です。
ルイス構(gòu)造における電子対とは、結(jié)合電子対(共有された電子)と孤立電子対(非結(jié)合電子)のことです。CH3 の炭素原子の周りには4つの電子対(3つの結(jié)合電子対と1つの孤立電子対)があります。
ルイス構(gòu)造において、點(diǎn)は価電子を表します。1つの點(diǎn)は1つの価電子を示します。CH3 の場合、炭素は3つの結(jié)合電子対(線)と1つの孤立電子対(點(diǎn)2つ)に囲まれています。これにより、原子間での電子の共有や非共有を視覚的に理解できます。
 |