
ルイス構(gòu)造は、ギルバート?N?ルイスによって考案され、分子における電子配置を視覚的に表すものです。価電子をドットで、結(jié)合をラインで描き、ルイス構(gòu)造は八隅則に基づいて分子の形狀や特性を予測(cè)します。この規(guī)則によれば、原子は外部殻層に8つの電子を持つことで安定性を達(dá)成しようとします。ルイス構(gòu)造はこの規(guī)則に従い、化學(xué)結(jié)合の明確な畫像を提供します。
五フッ化塩素(ClF5)は、塩素原子1つとフッ素原子5つが結(jié)合した無色無臭の気體です。ロケット推進(jìn)剤や化學(xué)合成におけるフッ素付加剤としてさまざまな用途を持っています。ClF5は過剰価化合物であり、三格二面角幾何學(xué)的形狀を持っています。

では、ClF5のルイス構(gòu)造を描いてみましょう:
ステップ1: 中心原子の特定:塩素(Cl)は、フッ素よりも電気陰性度が低いので、ClF5の中核原子です。
ステップ2: 全ての価電子數(shù)を計(jì)算:塩素は7つの価電子を供給し、各フッ素は7つ供給するため、合計(jì)は7 + (5 x 7) = 42価電子になります。
ステップ3: 電子を原子の周りに配置:各フッ素原子を中心の塩素原子に単結(jié)合(線)で結(jié)び、殘りの電子を各フッ素原子の周囲に一人対として配置します。
ステップ4: 八隅則を満たす:各フッ素原子には8つの電子(2つの一人対と1つの結(jié)合対)、そして塩素原子には10つの電子(2つの一人対と5つの結(jié)合対)があることを確認(rèn)します。
ステップ5: 形式電荷をチェック:形式電荷は必要ないかもしれません。なぜなら、すべての原子が八隅則または塩素の場(chǎng)合の準(zhǔn)八隅則を達(dá)成しているからです。
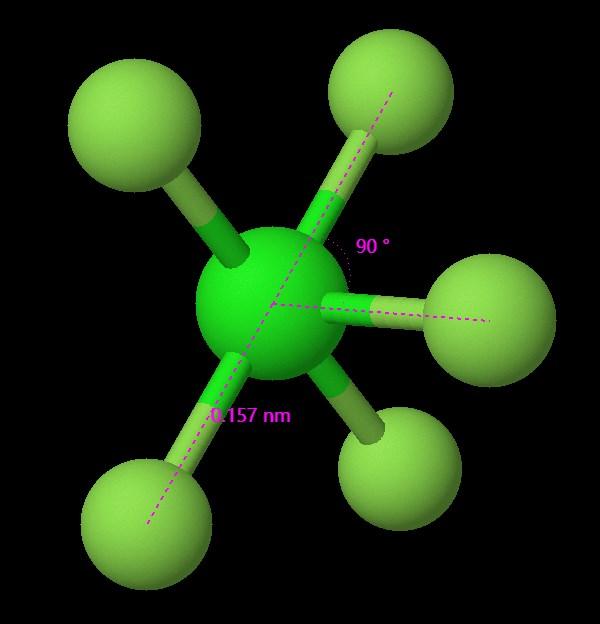
五フッ化塩素の構(gòu)造は、中心の塩素原子の周りに10個(gè)の電子または5つの電子対があり、一人対がないため、ClF5の分子幾何學(xué)は三格二面形となります。F-Cl-F結(jié)合間には異なる結(jié)合角があります。
この理論は、電子反発と化合物が安定な形態(tài)を取る必要性について説明しています。ClF5では、塩素とフッ素の間に5つのシグマ結(jié)合が形成され、各フッ素原子には3つの一人対があります。塩素は7つの価電子しか持っていないにもかかわらず、ルイス構(gòu)造は5つの結(jié)合対を示しており、これがd軌道の使用を示唆しています。しかし、高度な計(jì)算では、電子構(gòu)造は実際にはd軌道を含む5つの明確な結(jié)合ではなく、6つの原子全體にわたって5つの分散結(jié)合であることがわかります。
ルイス構(gòu)造は、ClF5が三格二面形幾何學(xué)を採用することを示唆しています。この配列では、5つのフッ素原子は中心の塩素原子の周りに対稱的に配置され、5つの結(jié)合対が形成されます。この幾何學(xué)は電子-電子反発を最小限に抑え、安定した構(gòu)成をもたらします。
塩素とフッ素分子の相互作用中に形成される軌道と結(jié)合を調(diào)べることで、五フッ化塩素の混合狀態(tài)を決定します。関與する軌道は、3s、3py、3px、3pz、3dx2–y2、および3dz2です。基底狀態(tài)にある中心原子である塩素原子は、その形成において3s23p5の構(gòu)成を持ちます。
基勵(lì)狀態(tài)では、3sおよび3px軌道內(nèi)の電子対はペアとなり、それぞれのペアの1つが未占有の3dz2および3dx2-y2軌道に促進(jìn)されます。これにより、全ての5つの半分に満たされた軌道(1つの3s、3つの3p、1つの3d)が混合し、5つのsp3d混合軌道が生成されます。
ClF5の結(jié)合角は約90度および120度です。これは分子の三格二面形幾何學(xué)から生じるもので、5つのフッ素原子が正三角二面體の頂點(diǎn)に位置し、隣接するフッ素原子間で異なる結(jié)合角が形成されます。ClF5の結(jié)合長は約182 pmです。
| 五フッ化塩素 Cas 7790-89-8 | |
| 分子式 | ClF5 |
| 分子形狀 | 三格二面形 |
| 極性 | 極性あり |
| 混合 | sp3d混合 |
| 結(jié)合角 | 90度と120度 |
| 結(jié)合長 | 182 pm |
ルイス構(gòu)造が極性かどうかを判斷するには、分子幾何學(xué)と結(jié)合極性を検討します。五フッ化塩素(ClF5)の場(chǎng)合、ルイス構(gòu)造は中心の塩素に5つのフッ素原子が結(jié)合していることを示しています。ClF5は三格二面形の幾何學(xué)を持ち、5つのフッ素原子が塩素原子の周りに対稱的に配置されています。電子密度分布の非対稱性により、ClF5は極性分子です。
ClF5の総結(jié)合エネルギーを計(jì)算するには、まず単一の塩素-フッ素(Cl-F)結(jié)合の結(jié)合エネルギーを調(diào)べます。それは約270 kJ/molです。ClF5には5つのCl-F結(jié)合があるため、1つのCl-F結(jié)合の結(jié)合エネルギーに結(jié)合の數(shù)を掛けます。これにより、ClF5の総結(jié)合エネルギーは1350 kJ/molとなります。この値は、1モルのClF5分子中の全てのCl-F結(jié)合を破壊するために必要なエネルギーを表します。
結(jié)合順位は、原子対間の化學(xué)結(jié)合の數(shù)です。ClF5のルイス構(gòu)造では、各塩素-フッ素結(jié)合は単結(jié)合なので、各Cl-F結(jié)合の結(jié)合順位は1です。共振構(gòu)造を持つ分子の場(chǎng)合、結(jié)合順位は異なる構(gòu)造の平均ですが、ClF5には共振がないため、結(jié)合順位は1のままです。
ルイス構(gòu)造における電子群には、共有電子対(結(jié)合対)と一人対(非結(jié)合電子)が含まれます。ClF5では、各塩素原子の周りに5つの電子群があり、これは5つのCl-F結(jié)合(5つの結(jié)合対と塩素上の一人対なし)に対応します。
ルイスドット構(gòu)造では、ドットは価電子を表します。各ドットは1つの価電子に対応します。ClF5では、塩素は5つの結(jié)合対(ルイス構(gòu)造では線で表現(xiàn))に囲まれており、各フッ素原子は3対のドット(一人対)と塩素との1つの結(jié)合対を持っています。ドットは、電子がどのように共有されたりペアになったりするかを視覚化するのに役立ちます。
 |