El yoduro de potasio es una sal de yoduro metálico con el ion K(+). Actúa como eliminador de radicales libres y expectorante, siendo utilizado en solución saturada (SSKI) para tratar emergencias médicas como la crisis tirotoxica. Además, se emplea en situaciones de contaminación radiactiva con yodo y preparación preoperatoria para pacientes con hipertiroidismo.
El yoduro de potasio es un compuesto iónico compuesto por los iones K+ y I-. Cristaliza en estructura similar al cloruro de sodio y se produce industrialmente tratando KOH con yodo. Es un compuesto blanco de alta importancia comercial en la producción de aproximadamente 37,000 toneladas en 1985. Es menos higroscópico que el yoduro de sodio, facilitando su uso.
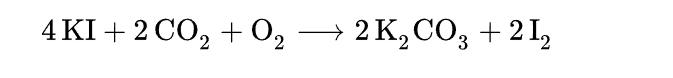
Dado que el ion yoduro es un agente reductor suave, I- puede ser fácilmente oxidado a yodo (I2) por oxidantes fuertes como el cloro:
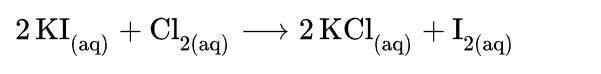
Este tipo de reacción se emplea en la extracción de yodo de fuentes naturales. La oxidación del yoduro por el aire produce un extracto púrpura al lavar muestras envejecidas de KI con diclorometano. El ácido yodhídrico (HI) formado en condiciones ácidas es un reductor aún más potente.
Al igual que otros yoduros, el KI forma triyoduros al combinarse con yodo elemental.
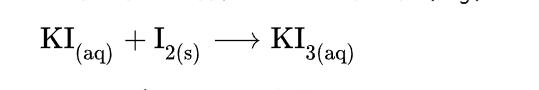
A diferencia de I2, los triyoduros de I3- son altamente solubles en agua. Esta reacción permite el uso del yodo en titulaciones redox. El KI3 acuoso, conocido como solución de Lugol, se utiliza como desinfectante y grabador de superficies metálicas.
El yoduro de potasio y el nitrato de plata se utilizan para fabricar yoduro de plata (I), empleado en películas fotográficas de alta velocidad y en la modificación artificial de precipitaciones:
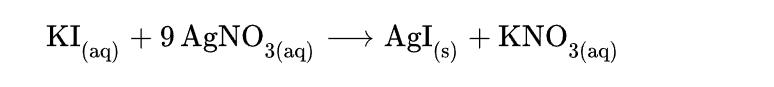
El KI es una fuente de yoduros en síntesis orgánica. Una aplicación útil es la preparación de yoduros de arilo a partir de sales de arilazolium.
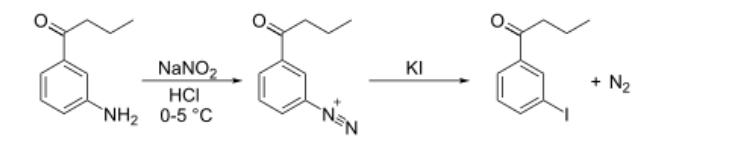
El KI, como fuente de yoduros, también puede actuar como catalizador nucleofílico en la alquilación de cloruros, bromuros o mesilatos de alquilo.
A temperatura ambiente, una solución de H2O2 parece no reaccionar y es extremadamente lenta. Sin embargo, al a?adir yoduro de potasio, el catalizador muestra un impacto significativo en la velocidad de descomposición del H2O2. El cambio de color indica que el KI vuelve a su estado original sin consumirse. La mezcla resultante genera una gran cantidad de espuma, conocida como "pasta de dientes de elefante". Experimentalmente:
A. La liberación rápida de oxígeno se debe a esta reacción:
B. En presencia de iones yoduro, la descomposición del peróxido de hidrógeno ocurre en dos etapas:
Cuando se mezcla peróxido de hidrógeno (H2O2) con yoduro de potasio (KI) en presencia de detergente, ocurre una reacción química llamada "pasta de dientes de elefante". En esta reacción, el peróxido de hidrógeno se descompone rápidamente (catalizada por el yoduro de potasio) en agua (2H2O) y oxígeno (O2). La presencia del detergente ayuda a capturar el oxígeno en forma de burbujas de jabón.
El material espumoso generado es el resultado de la rápida descomposición del peróxido de hidrógeno catalizada por el yoduro de potasio, liberando una gran cantidad de oxígeno. El jabón en la mezcla captura este gas, formando una torre de espuma que a menudo se describe como parecida a la pasta de dientes exprimida de un tubo, de ahí el nombre "pasta de dientes de elefante".
(1) Pueden surgir síntomas como náuseas, vómitos, dolor abdominal, diarrea, sabor metálico en la boca, fiebre, dolor de cabeza o acné. Si estos síntomas persisten o empeoran, informe inmediatamente a su médico o farmacéutico.
(2) Si su médico le ha indicado usar este medicamento, recuerde que él ha determinado que los beneficios para usted superan el riesgo de efectos secundarios. Muchas personas que usan este medicamento no tienen efectos secundarios graves.
(3) Si experimenta efectos secundarios graves, informe inmediatamente a su médico, como ardor en la boca/garganta, dolor en los dientes/encías, hinchazón en la boca, aumento de saliva, irritación ocular/párpados hinchados, dolor de cabeza intenso, hinchazón en el cuello/garganta (bocio), signos de función tiroidea baja (como aumento de peso, intolerancia al frío, latidos cardíacos lentos/irregulares, estre?imiento, fatiga inusual), confusión, entumecimiento/picazón/dolor/debilidad en manos/pies.
(4) Si experimenta efectos secundarios muy graves, busque atención médica de inmediato, como dolor en el pecho, heces negras, vómitos que parecen café molido, diarrea con sangre.
(5) Las reacciones alérgicas graves a este medicamento son raras. Sin embargo, si nota síntomas de una reacción alérgica grave, como sarpullido, picazón/hinchazón (especialmente en cara/lengua/garganta), mareos graves, dificultad para respirar, fiebre y dolor en las articulaciones, busque atención médica de inmediato.
Es crucial seguir estrictas medidas de seguridad al procesar KI para evitar la contaminación y garantizar su eficacia.
El almacenamiento y procedimientos de manejo son fundamentales. Los comprimidos de KI deben mantenerse en su envase original, en un lugar fresco y seco, fuera del alcance de los ni?os y mascotas. Evite el contacto con humedad y altas temperaturas.
Si entra en contacto con KI, lave bien el área afectada con agua y jabón. En caso de ingestión accidental de KI, llame al centro de control de intoxicaciones o busque atención médica inmediatamente.
En resumen, el yoduro de potasio muestra una variedad de usos y importancia en reacciones químicas, incluyendo su papel como fuente de yodo y su función en síntesis orgánica y ciencia de materiales. Para obtener más información sobre las propiedades químicas y aplicaciones prácticas del yoduro de potasio, se recomienda visitar la plataforma Guidechem para una investigación más profunda y obtener información relevante.
[1] https://brainly.com/question/41515423
[2] https://rutchem.rutgers.edu/cldf-demos/1019-cldf-demo-elephant-toothpaste
[3] http://www.vikit.cn/msds/
[4] https://pubchem.ncbi.nlm.nih.gov/compound/4875
[5] https://en.wikipedia.org/wiki/Potassium_iodide
[6] https://www.webmd.com/drugs/2/drug-1823/potassium-iodide-oral/details
[7] https://sciencedemonstrations.fas.harvard.edu/presentations/hydrogen-peroxide-decomposition-iodide
 |
 |
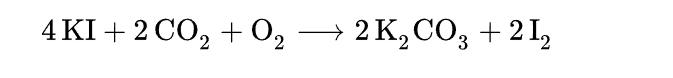 |